【要点】
○標的酵素を発現する領域のみを特異的に染色可能なラマンプローブの開発に成功
○酵素反応に伴う凝集体形成によって細胞内に滞留するプローブ分子を設計
○生体組織内における複数の酵素活性パターンを検出する技術への発展に期待
【概要】
東京工業大学 生命理工学院 生命理工学系の神谷真子教授と藤岡礼任助教ら、東京大学 大学院工学系研究科/東京大学 先端科学技術研究センターの小関泰之教授ら、理化学研究所 生命機能科学研究センターの小幡史明チームリーダーらの研究チームは、標的酵素との反応後に凝集体を形成することによって標的酵素の発現領域と非発現領域を染め分け可能な新規activatable型ラマンプローブ(用語1)の開発に成功した。
ラマン顕微法(用語2)は蛍光法と比べて多重検出能に優れており、一度に複数の標的を可視化できるイメージング手法として注目を集めてきた。しかし、特定の条件下でのみラマン信号を発するactivatable型ラマンプローブの開発例は少なく、可視化できる対象には制限があった。本研究では、さまざまな性質の細胞が混在して存在するヘテロな生体組織環境においても標的酵素の発現領域のみを選択的に検出可能なラマンプローブを設計・開発した。このプローブは、標的酵素と反応すると凝集体を形成しやすくなる性質を持つため滞留性が高く、細胞外に漏れ出しにくい。そのため、標的細胞選択的に高強度のシグナルを得ることができる。酵素活性を検出する技術は術中におけるがん部位の可視化に有用であることが知られているため、開発した設計法により、生体組織内で複数の酵素活性を同時検出可能なプローブ群を開発できれば、より高い精度でがんを可視化する技術の確立につながると期待される。
本研究成果は、4月14日付の「Journal of the American Chemical Society」に掲載された。
●背景
分子振動の情報を直接検出することができるラマン顕微法は、現在の生命科学研究で汎用されている蛍光法と比べて多重検出能が高いことが特徴である。すなわち、一度に複数の標的分子を可視化可能なイメージング手法として近年注目されている。一方で、このようなラマン顕微法に用いることのできるラマンプローブのうち、標的分子と反応することでラマン信号強度が変化する機能性を有するラマンプローブの開発例は限られていた。
当研究チームでは、これまでに、標的分子である酵素との反応に伴う吸収波長変化によって前期共鳴ラマン効果(用語3)が増大することを利用してラマン信号をoffからonへと変化させることができるactivatable型ラマンプローブを世界に先駆けて開発し、生きた細胞で酵素活性を検出することに成功してきた。しかし、開発したプローブの細胞内滞留性が乏しく、酵素反応後に標的細胞から漏れ出してしまう性質があったため、さまざまな細胞が混在する生体組織においては目的の細胞のみを特異的に検出することができないという課題があった。
●研究成果
本研究ではまず、キサンテン環 (用語4)の 9位にCN基を有するロドール誘導体(用語5)が水溶液中で高い凝集性を示すことを見出した。さらに、このような高い凝集性は中性条件下の双性イオン(用語6)型構造に特徴的なものであり、類似の構造を有するカチオン(用語7)性の誘導体では凝集が起こりづらいことを明らかとした。
そこで、この現象を利用して、酵素反応前はカチオン型となっているため凝集性が起こりづらいが、酵素反応後には双性イオン型となって凝集性を持つようになることで細胞内滞留性が向上する新規activatable型ラマンプローブ(図1)の開発を行った。さらに、開発したプローブは酵素反応前後で吸収波長が変化するため、前期共鳴ラマン効果によって1分子あたりのラマン信号強度も増大する性質がある。この凝集性と前期共鳴ラマン効果の相乗効果により、酵素反応後に強いラマン信号を発生する。ショウジョウバエ遺伝学を用い、開発したラマンプローブの生体応用可能性について検証した。誘導ラマン散乱顕微法(用語8)により、ショウジョウバエ組織の観察を行ったところ、標的酵素発現領域のみを高選択的かつ高感度に検出することに成功した(図2)。
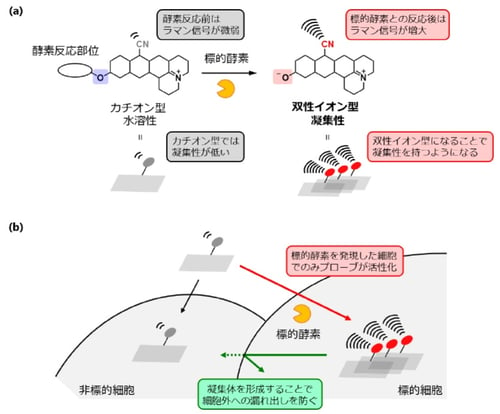
図1 酵素反応に伴う凝集体形成を利用した標的細胞の特異的検出
(a) 今回デザインしたプローブの特徴 (b) 標的細胞検出メカニズムのイメージ
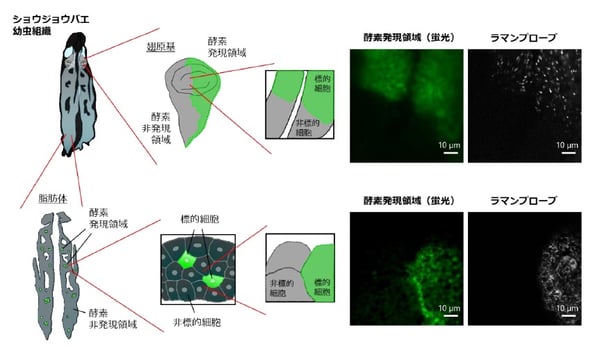 図2 開発したラマンプローブとショウジョウバエ遺伝学を応用した
図2 開発したラマンプローブとショウジョウバエ遺伝学を応用した
標的酵素発現領域の特異的検出
●社会的インパクト
酵素との反応によってはじめて蛍光を発するactivatable型蛍光プローブは、がん細胞に特徴的な酵素を標的とすることができる。そのため、がん細胞を特異的に検出可能な技術としての利用が注目されており、術中でのがんイメージングにも有効であることが報告されている。検出標的とする酵素の種類を増やすことができれば、より精度の高いがんイメージングが行えると考えられるが、蛍光イメージングには色数の壁(用語9)があり、一度に多数の酵素活性を検出することは困難である。一方でラマン顕微法は蛍光法と比べて多重検出能が高いため、ラマンプローブを用いることで多数の酵素活性を同時に検出できる可能性がある。本研究で開発したラマンプローブは生体組織においても標的酵素発現領域を特異的に検出可能であったため、複数の酵素を標的としたラマンプローブ群を用いた高精度ながんイメージングへの応用などが期待される。
●今後の展開
本研究においては、ショウジョウバエ組織を用いることでプローブの概念実証を行ったが、今後は哺乳類の生体組織にも適用することでプローブの利用可能性を拡大していく。また、凝集体形成を活用した本プローブの分子設計戦略は、全く新しいデザインのラマンプローブ開発につながる知見になると考えられ、今後のラマンイメージング技術の発展を加速させるものであると期待される。
●付記
本研究は、科学研究費助成事業 学術変革領域(B)「機能性ラマンプローブによる革新的多重イメージング(革新ラマン)」(JP20H05724、JP20H05725、JP20H05726)の研究の一環として行われた。
【用語説明】
(1) ラマンプローブ:ラマン散乱により検出可能な特有の分子振動を有する分子の総称。異なる分子振動周波数を有するラマンプローブを用いることで、複数種の分子の多重検出が可能となる。
(2) ラマン顕微法:光と分子の相互作用の一つであるラマン散乱を検出することによる顕微法。ラマン散乱光は入射光に対して分子の振動数分だけ振動数が低下し、長波長化した光として生じるため、これを検出することで試料に含まれる分子の構造解析を行うことができる。
(3) 前期共鳴ラマン効果:共鳴ラマン効果の一つであり、分子の吸収波長よりやや長波長の励起光を照射することで、通常のラマン散乱よりも散乱強度が増大する現象。共鳴効果は分子の波長が長くなるにしたがって非線形的に増大する性質があり、分子の吸収波長を制御することでラマン信号強度も制御することができる。
(4) キサンテン環:アントラセンの中心のベンゼン環をピラン環に置き換えた3環構造を有する有機化合物の総称。
(5) ロドール誘導体:キサンテン構造を有するローダミン色素の片方のアミノ基をヒドロキシ基に置換した有機化合物の総称。
(6) 双性イオン:プラスとマイナスの電荷を併せ持った分子。
(7) カチオン:プラスの電荷を持った分子。
(8) 誘導ラマン散乱顕微法:2色のパルスレーザーを用いた高速ラマンイメージング法の一つ。
(9) 色数の壁:蛍光スペクトルの幅の広さのために、同時に検出可能な色の数に限度(color barrier)があること。一般的に5~6色が蛍光法の同時検出数の限界であるとされている。
【論文情報】
掲載誌:Journal of the American Chemical Society
論文タイトル:Activatable Raman Probes Utilizing Enzyme-Induced Aggregate Formation for Selective Ex Vivo Imaging
著者:Hiroyoshi Fujioka, Minoru Kawatani, Spencer John Spratt, Ayumi Komazawa, Yoshihiro Misawa, Jingwen Shou, Takaha Mizuguchi, Hina Kosakamoto, Ryosuke Kojima, Yasuteru Urano, Fumiaki Obata, Yasuyuki Ozeki and Mako Kamiya
DOI:10.1021/jacs.2c12381
プレスリリース本文:PDFファイル
Journal of the American Chemical Society:https://pubs.acs.org/doi/10.1021/jacs.2c12381
おすすめ記事
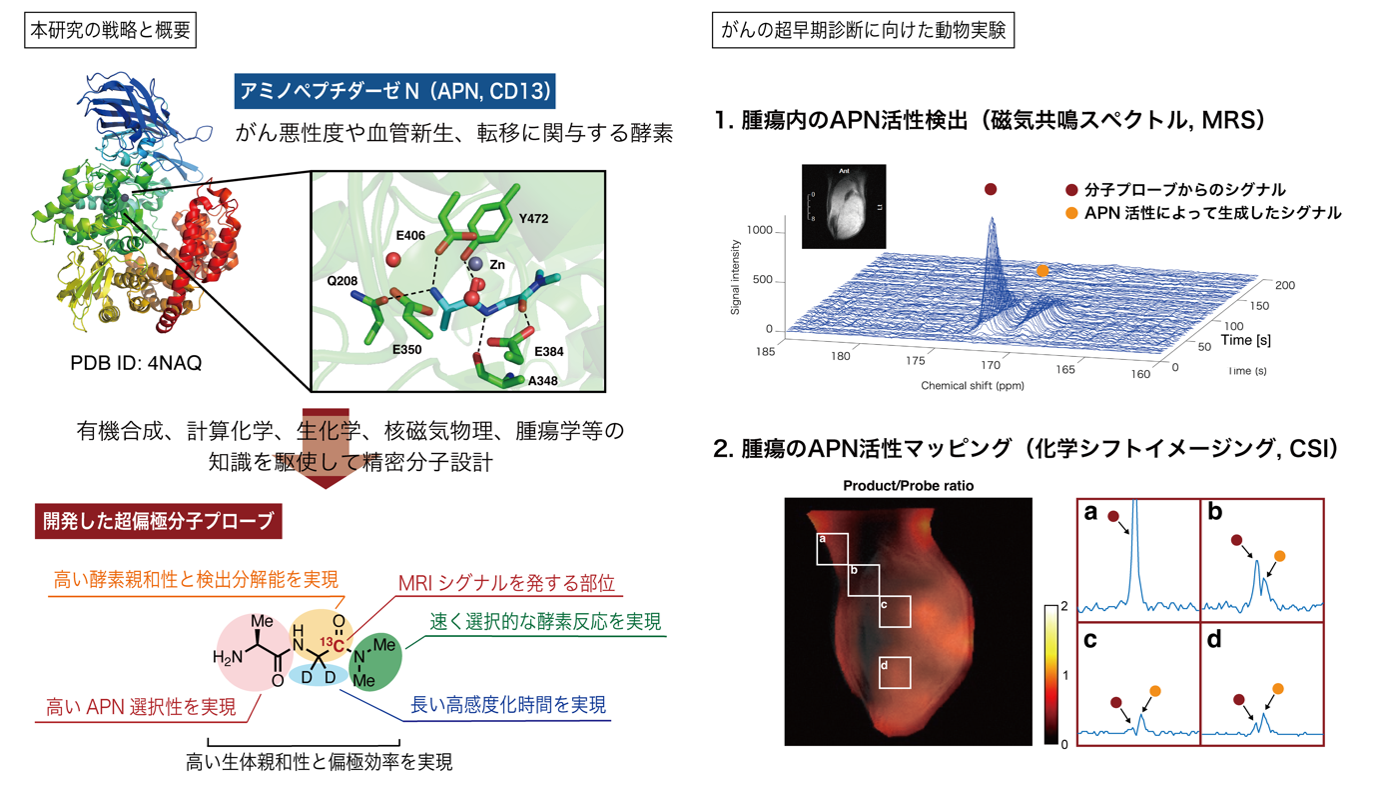
精密分子設計による高感度MRI分子プローブの開発 〜早期診断に向けたがん関連酵素活性の生体内リアルタイム計測〜
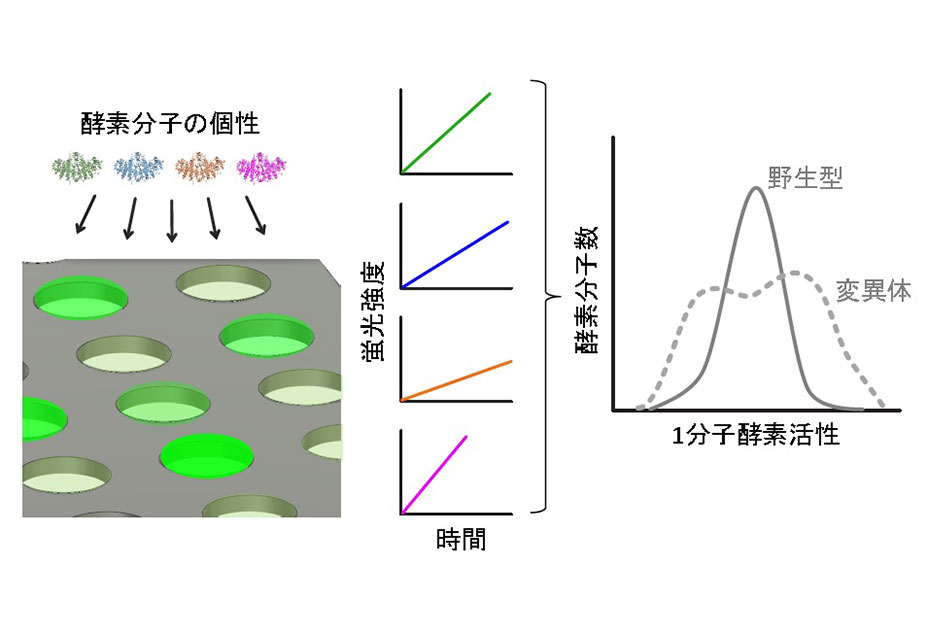
酵素の分子個性のダイバーシティは酵素進化のバロメーターとなる