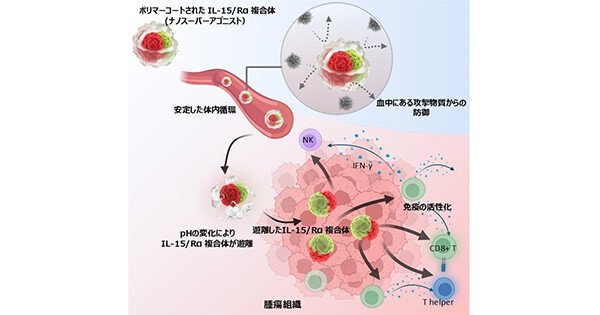
⚫免疫細胞の浸潤性が悪い難治性のがん(Cold Tumor)に対する新たな免疫療法として独自に開発したインターロイキン 12 (IL12) 搭載ナノマシン(ナノサイトカイン)の応用を検討した。
⚫免疫チェックポイント阻害剤と IL12 搭載ナノマシンの併用により、悪性度の高いがんとして知られるメラノーマ(悪性黒色腫)およびトリプルネガティブ乳がん(TNBC)のモデルマウスで完全奏効(CR)を実現した。
⚫IL12 は、古くから知られる炎症性サイトカインのひとつで、その免疫細胞誘導力の強さから、がん免疫療法への応用が検討されてきたが、その高い毒性の制御が難しく、臨床への応用は進んでいない。
⚫腫瘍内部において、がん細胞の活性度合いが高いほど酸性に傾く傾向があるため、pH の低下に応じて IL12 を放出するリンカーを使用することで、腫瘍内の時間的空間的変化に応じた治療が可能となった。
⚫IL12 製剤の 2 回目投与で、しばしば観察される炎症抑制性のインターロイキン 10(IL10)の発現が、本製剤では見られなかった。
⚫この時空間的制御(Spatiotemporal Control)により、免疫抵抗性TNBCにおけるIL12の有効量を従来の 1/10 にまで下げることが可能となった。また、MTD(最大耐量:これ以上の量の投与は死を招くことを意味する)について、ヒトの臨床試験で報告されている IL12 の量の千倍相当量でも毒性は確認できなかった。
⚫本発表は、東京大学大学院工学系研究科のオラシオ・カブラル准教授(iCONM 客員研究員)のグループ、東京大学病院の垣見和宏・特任教授(免疫細胞学)および iCONM とともに共同で進める難治性がんの攻略プロジェクト。論文の詳細は以下のサイトを参照。
P.Chen, W.Yang, K.Nagaoka, G.L.Huang, T.Miyazaki, T.Hong, S.Li,K.Igarashi, K.Takeda, K.Kakimi*, K.Kataoka* and H.Cabral*, Advanced Science, in press.
DOI: https://doi.org/10.1002/advs.202205139
公益財団法人川崎市産業振興財団 ナノ医療イノベーションセンター(センター長:片岡一則、所在地:川崎市川崎区、略称:iCONM)は、同センターのオラシオ・カブラル客員研究員(東京大学大学院工学系研究科バイオエンジニアリング専攻 准教授)のグループおよび東京大学病院の垣見和宏・特任教授(免疫細胞学)との共同研究成果として、「IL-12 搭載ナノマシン(ナノサイトカイン)が、炎症反応の時間的空間的制御を介した抗腫瘍免疫作用により、進行した cold tumor(注1) を安全に駆逐するポテンシャルを有する」 と題する論文(注2)が 2/5 付 Advanced Science に掲載されたことを報告いたします。
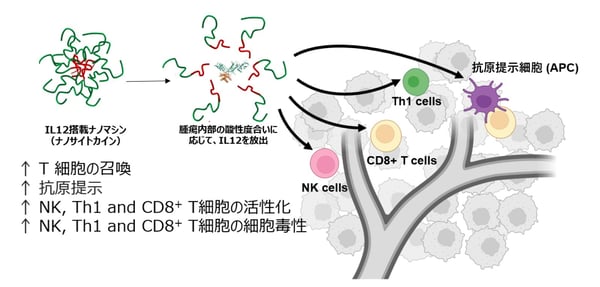
多くの固形がんは、免疫抵抗性の微小環境を持ち、免疫細胞の浸潤、活性化、エフェクター機能が阻害されるため、抗 PD-1 抗体や抗 CTLA-4 抗体を含む免疫チェックポイント阻害剤(ICI)による免疫療法に反応しない Cold Tumor と呼ばれる状態にあります。インターロイキン 12(IL-12)(注3)は、最も強い炎症性サイトカインの一つです。そのため、腫瘍の免疫力を高め、免疫療法の奏効率を高められるのではないかと期待されています。しかし、IL-12 は全身性の免疫活性化により非常に毒性が強く、安全な投与量での臨床効果は極めて限定的です。そこで、IL-12 の免疫活性化機能を腫瘍内部の部位における酸性度に基づき制御することで、腫瘍を標的とした免疫強化が可能な IL-12 搭載ナノマシン(ナノサイトカイン)を開発しました。このナノサイトカインは、pH 感応性高分子材料をベースに、腫瘍内の部位で異なる pH に応じて内含するサイトカインを放出することができます。その結果、IL-12 により引き起こされる全身性の副作用を回避することが可能となります。トリプルネガティブ乳がん(TNBC)モデルマウスでは、ナノサイトカインが免疫力を高め、腫瘍への免疫細胞の浸潤レベルを上昇させることが確認できました。また、ICI との相乗効果により、原発性および転移性腫瘍の両方において完全奏効(CR)を実現しました。
<本研究の新規性>
・IL-12 は古くから抗がん剤としての臨床応用が研究されていますが、その強い毒性と最大耐量下では十分な治療効果が得られないことが初期臨床試験で示され、その解決が求められています。今回独自に開発したナノサイトカインは、時空間的にサイトカインの放出を制御する IL-12 送達システムを実証した世界初の事例となります。
・本製剤は、健康な臓器と腫瘍の pH 差を感知することにより、IL-12 の生理活性を安定的に制御することができます。
・IL-12 による免疫反応を時空間的に制御することができ、正常組織では、標的外の免疫活性化と反作用が減少し、一方、腫瘍組織では炎症反応が増強されることが示されました。
・免疫抵抗性を持つ Cold Tumor に対し、遺伝子発現レベルで免疫細胞の浸潤性を高め、強い炎症反応を起こさせることができるため、ICI との相乗効果で進行した原発性および転移性腫瘍を完全に根絶することが可能です。
<本研究の重要性と既存の治療法との比較>
IL-12 は最も強い炎症性サイトカインの一つです。そのため、腫瘍組織に炎症を起こさせ、免疫療法の奏効率を高めるために使用できないかと以前より大きな関心が持たれています。しかしながら、IL-12は全身性の免疫活性化により極めて毒性が強く、最大耐量(MTD)(注 4)であっても臨床効果は極めて限定的であることが分かっています。IL-12 の安全性と腫瘍選択性を高めるために、様々な研究機関で IL-12タンパク質をデザインする試みに大きな努力が払われていますが、現状では、依然として良好な結果は得られておらず、IL-12 の問題を克服するには至っていません。また、このようなタンパク工学システムにおける炎症動態はまだ十分に理解されておらず、反作用的な副次反応についても不明なままです。IL-12 を搭載したナノマシン(ナノサイトカイン)は、腫瘍組織への高い集積性、選択的な腫瘍内免疫活性、制御された全身性免疫との相互作用により、炎症の時空間的制御を可能にし、上記の問題を一度に解決することができます。例えば、IL-12 単体や標準的な IL-12 製剤(融合タンパク質やイムノサイトカインなど)で、2 回目の注入後によく見られる炎症抑制性のインターロイキン-10(IL-10)(注3)の発現も制御可能です。このような時空間制御は、抗腫瘍効果を低下させることなく反復投与スケジュールを実現する上で有利に働くと考えられます。また、炎症を起こさせる部位を限定できることで、IL-12 の有効治療域(注5)を拡大することが可能となりました。このように、ナノサイトカインは、逆作用する免疫反応をブロックすることで、免疫抑制性のトリプルネガティブ乳がんに対する有効投与量を 10 分の 1 に減少させることができました。さらに、ヒト試験で報告されているネイティブ IL-12の MTD の 1,000 倍の用量でも毒性は確認されず、安全性が向上しました。ナノサイトカインは、免疫抑制性腫瘍に強い炎症を起こさせ、また、有効性を阻害する逆反応の回避も実現しました。これにより、本製剤は、免疫抑制性腫瘍の微小環境を逆転させることにより、免疫チェックポイント阻害剤(ICI)との強い相乗効果を示すに至りました。
注目すべきは、本製剤が生体適合性のある FDA 認可の材料に基づいているため、この戦略は臨床への応用にも適用しやすいところにあります。さらに、他の治療用タンパク製剤にも応用可能な技術であり、腫瘍をターゲットとした生物製剤送達に向けた実用的な戦略として機能すると考えています。
注1)Cold Tumor:免疫細胞が浸潤しにくく、そのため炎症反応が起きずに活性を保つことができる腫瘍のこと。逆に、炎症が起きやすい腫瘍を Hot Tumor という。炎症反応が起きないため難治性となる。
注2)P. Chen, W.Yang, K.Nagaoka, G.L.Huang, T.Miyazaki, T.Hong, S.Li, K.Igarashi, K.Takeda, K.Kakimi*, K.Kataoka* and H.Cabral*, Advanced Science, in press.
DOI: https://doi.org/10.1002/advs.202205139
注3)インターロイキン:サイトカイン(細胞が分泌する生理活性低分子タンパク質)のうち、免疫に関係するものをインターロイキン(IL)として分類し、現在、30 種類以上が特定されている。なかでも、IL12 は、NK(ナチュラルキラー)細胞など抗腫瘍免疫担当細胞を活性化し、腫瘍組織での炎症を引き起こす。その炎症反応によりがん細胞はダメージを受けて弱まる。それに対して、IL10 は、炎症性サイトカインの産生を阻害する作用があり、抗炎症作用を持つ。がん免疫療法を効果的に行うには、IL12 を増やし、IL10 を減らす必要があるものの、IL12の有効治療域は狭く、副作用の制御が大きな課題となっている。
注4)MTD:最大耐量。生命が耐えられる最大の投与量。これ以上の量の投与は致死量となる。
注5)有効治療域:最小有効血中濃度(この濃度未満では有効性が示されない)と最小中毒濃度(この濃度以上では、深刻な副作用を生じる)の間の血中濃度範囲。
Advanced Science 誌について
材料科学、物理学、化学、医学、生命科学、工学の基礎および応用研究をカバーする誰でも無料で閲覧できる国際的学術誌です。直近のインパクトファクター (IF) は、15.622。厳正な審査によって選ばれた最先端の研究を、最高品質の制作基準を用いて掲載し、プレミアム・オープンアクセス・ジャーナルを実現しています。最先端の科学に誰もが手軽にアクセスできることが、この活気ある革新的な同誌の目的です。
ISSN: 2198-3844(オンライン)。CODEN:ASDCCF。年間 36 号発行。
Overview - Advanced Science - Wiley Online Library
公益財団法人川崎市産業振興財団について
産業の空洞化と需要構造の変化に対処する目的で、川崎市の 100%出捐により昭和 63 年に設立されました。市場開拓、研究開発型企業への脱皮、それを支える技術力の養成、人材の育成、市場ニーズの把握等をより高次に実現するため、川崎市産業振興会館の機能を活用し、地域産業情報の交流促進、研究開発機構の創設による技術の高度化と企業交流、研修会等による創造性豊かな人材の育成、展示事業による販路拡大等の事業を推進し、地域経済の活性化に寄与しています。
https://www.kawasaki-net.ne.jp/
ナノ医療イノベーションセンターについて
ナノ医療イノベーションセンター(iCONM)は、キングスカイフロントにおけるライフサイエンス分野の拠点形成の核となる先導的な施設として、川崎市の依頼により、公益財団法人川崎市産業振興財団が、事業者兼提案者として国の施策を活用し、平成 27 年 4 月より運営を開始しました。有機合成・微細加工から前臨床試験までの研究開発を一気通貫で行うことが可能な最先端の設備と実験機器を備え、産学官・医工連携によるオープンイノベーションを推進することを目的に設計された、世界でも類を見ない非常にユニークな研究施設です。
https://iconm.kawasaki-net.ne.jp/
東京大学大学院工学系研究科バイオエンジニアリング専攻について
バイオエンジニアリング専攻は、少子高齢化が進み、持続的発展を希求する社会において、人類の健康と福祉の増進に貢献することを目指します。本専攻では、この目的を達成するために、既存の工学及び生命科学ディシプリンの境界領域にあって両者を有機的につなぐ融合学問分野であるバイオエンジニアリングの教育・研究を推進します。バイオエンジニアリングの特徴は、物質・システムと生体との相互作用を理解・解明して学理を打ち立てるとともに、その理論に基づいて相互作用を制御する基盤技術を構築することにあります。生体との相互作用を自在に制御することで、物質やシステムは人間にとって飛躍的に有益で優しいものに変身し、革新的な医用技術が生まれることが期待されます。このようなバイオエンジニアリングの教育・研究を通じて、バイオメディカル産業を先導し支える人材を輩出するとともに、予防・診断・治療が一体化した未来型医療システムの創成に貢献することを目指します。
http://www.bioeng.t.u-tokyo.ac.jp/
カブラル オラシオ | 東京大学大学院工学系研究科バイオエンジニアリング専攻 (u-tokyo.ac.jp)
プレスリリース本文:PDFファイル
Advanced Science:https://onlinelibrary.wiley.com/doi/10.1002/advs.202205139
おすすめ記事
本件に関連する記事はこちら
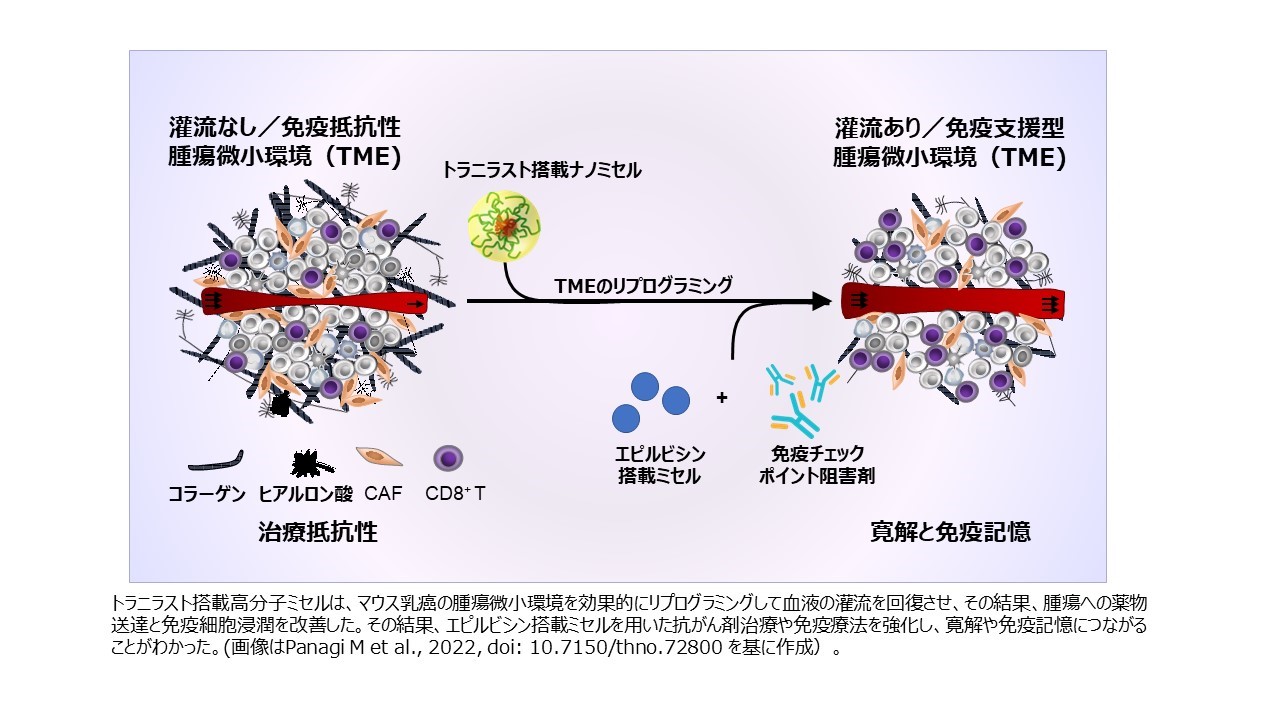
難治性がんのシールドを破壊し、 薬剤や免疫細胞が浸透しやすくする技術の開発 ~ Nature Communications に掲載~
悪性脳腫瘍の中で特異的に活性化し、副作用なく治療を行う免疫チェックポイント阻害抗体の開発に成功