発表のポイント
◆ ヒト細胞およびマウス組織のtRNAにおいて、脱硫型修飾(xm5h2U)が内在的に生成されていることを初めて実証しました。◆ 脱硫型修飾は特定のtRNAのアミノアシル化効率とコドン解読能を低下させ、タンパク質合成効率を制御することを明らかにしました。
◆ クライオ電子顕微鏡を用いた構造解析により、脱硫型修飾を有するtRNAがリボソーム上で対応するコドンを認識しにくくなることを明らかにしました。

概要図:脱硫型tRNA修飾による翻訳制御機構
概要
東京大学大学院工学系研究科の莫 喩楓(Yufeng Mo) 大学院生と鈴木 勉 教授の研究グループは、脱硫(元素記号がSである、硫黄を含む分子が離脱する反応)したtRNA(注1)修飾による翻訳制御機構を解明し、その機構が酸化ストレス(注2)応答と関連する可能性を示しました。
タンパク質合成においてアダプター分子として機能するtRNAのアンチコドン(注3)には、さまざまな化学修飾が施されており、翻訳の正確性と効率を適切に制御しています。tRNAには多様な化学修飾が存在しますが、その中でもアンチコドンの1塩基目に位置する5-メチル-2-チオウリジン誘導体(xm5s2U)は、リボソーム(注4)上でmRNAのコドン(注5)を正確に解読するうえで重要な役割を担っています。
本研究では、ヒト細胞およびマウス組織において、tRNAのxm5s2U修飾が細胞内で酸化的に脱硫され、4-ピリミジノン誘導体(xm5h2U)へと変換されることを明らかにしました。脱硫したtRNAではアミノアシル化(注6)効率が著しく低下し、さらにリボソーム上でのmRNAコドンの解読能も失われることが分かりました。その結果、タンパク質合成効率が低下することが示されました。
加えて、クライオ電子顕微鏡(注7)を用いた構造解析により、脱硫型修飾を有するtRNAがリボソーム上で対応するコドンを認識しにくくなることを明らかにしました。
これらの成果は、酸化ストレス条件下において、tRNA修飾の脱硫を介して翻訳を制御する新たな分子機構の存在を示すものです。
発表内容
〈研究の背景〉
生命活動は、精密な遺伝子発現制御によって維持されています。遺伝子発現は、遺伝情報が転写される段階だけでなく、タンパク質が合成される翻訳段階においても厳密に制御されています。翻訳の過程では、mRNAのコドンがリボソーム上でtRNAのアンチコドンによって読み取られ、この認識の正確さが正しいタンパク質合成を支えています。翻訳の精度は、生命の維持や環境変化への適応に直結する重要な要素です。
tRNAには多様な化学修飾が存在し、これらは翻訳の正確性と効率を制御するうえで重要な役割を担っています。特にアンチコドンの1字目(34位)に導入される修飾は、コドンとの結合様式に影響を与え、どのコドンをどの程度の効率で読み取るかを決定する鍵となります。このようなtRNA修飾による翻訳制御は、遺伝子発現を柔軟に調節する仕組みであり、細胞の恒常性維持やストレス応答など、さまざまな生命現象に深く関与しています。
2-チオウリジン(s2U)とその誘導体である5-メチル-2-チオウリジン誘導体(xm5s2U)は、アンチコドン34位に存在する主要な修飾の1つであり、ヒト細胞質ではtRNALysを含む4種類のtRNAに導入されています(図1A)。s2U修飾は、tRNAのアミノアシル化や、プリン塩基を3字目にもつコドン(NNRコドン)の正確かつ高効率な解読、さらにリボソームにおける転座反応(注8)など、翻訳過程において多面的な機能を果たします。
一方、s2U修飾は化学的に不安定であり、試験管内ではチオカルボニル基が酸化されることで容易に脱硫され、4-ピリミジノン(h2U)へと変換されることが知られています(図1B)。細胞内では活性酸素が恒常的に産生されていることから、s2Uの脱硫は酸化ストレスに伴って内在的に生じる可能性があります。そこで本研究では、RNA質量分析法(注9)を用いて、ヒト培養細胞およびマウス、ブタの組織由来tRNAを解析しました。その結果、5-メトキシカルボニルメチル-2-チオウリジン(mcm5s2U)や5-タウリノメチル-2-チオウリジン(τm5s2U)よりも分子量が32 Da(読みはダルトン、1Daは12C原子の質量の1/12)低い未同定ヌクレオシドを検出しました。この分子量差は硫黄原子が酸素原子に置換された場合に相当し、h2U誘導体が細胞内tRNAに実際に存在することを示唆しています。しかし、これらの脱硫tRNA修飾が翻訳制御においてどのような分子機構的役割を担うのかについては、これまで明らかにされていませんでした。
〈研究の内容〉
莫 喩楓 大学院生と宮内 健常 特任研究員らはまず、各種ヒト培養細胞やマウス肝臓などの哺乳動物組織からtRNAを単離精製し、RNA質量分析法を用いて、tRNAの修飾状態を分析しました。精密質量や衝突活性化解離(注10)により、細胞由来のtRNAにh2U修飾があることが同定されました(図1C)。修飾率は細胞の種類によって異なっていました。さらに、細胞からtRNAを精製する際に異なるs2U誘導体を有する大腸菌tRNAを内部標準として加えることで、h2U誘導体の形成が実験操作に由来する偽陽性ではないことが証明され、h2U修飾は細胞内に存在することが示されました。

図1:細胞内における脱硫型tRNA修飾の存在
(A)5-メチル-2-チオウリジン誘導体(xm5s2U)は、tRNAアンチコドン1字目に存在する主要な修飾の1つである。
(B)tRNA中のxm5s2Uの酸化脱硫反応。
(C)マウス組織において、細胞質tRNAおよびミトコンドリアtRNAに脱硫型tRNA修飾(xm5h2U)が異なる比率で存在する。
次に、兵庫県立大学の今高 寛晃 教授らが開発したヒト因子由来の再構成型タンパク質合成系を用いて、脱硫型修飾であるmcm5h2Uを有するtRNAの翻訳能を解析しました。その結果、脱硫化により翻訳活性が著しく低下することが明らかとなりました(図2A)。さらに、細胞抽出液のポリソーム画分(注11)においてmcm5h2U修飾を有するtRNAが検出され、脱硫したtRNAが細胞内で実際に翻訳に参加していることが強く示されました。
続いて、mcm5h2U修飾が翻訳過程のどの段階に影響を及ぼすのかを詳細に解析しました。まず、修飾状態の異なるtRNAを用いてアミノアシル化反応を行ったところ、mcm5s2U修飾を有するtRNAのうち、Gln、Glu、Lysに対応するtRNAでは、脱硫化によりアミノアシル化効率が顕著に低下することが明らかになりました(図2B)。一方、tRNAArgではアミノアシル化能に変化は認められませんでした。
さらに、リボソーム上でのコドン認識への影響を検討しました。通常のtRNALysはAAAおよびAAGコドンのいずれにも効率よく結合しましたが、脱硫化したtRNALysはAAAコドンにはほとんど結合せず、AAGコドンに対しても結合能が大きく低下していました(図2C)。これらの結果から、mcm5s2Uの脱硫は特定のtRNAにおいてアミノアシル化を阻害するとともに、コドン認識能力を低下させることが示されました。

図2:脱硫型tRNA修飾が翻訳過程に及ぼす影響
(A)脱硫型修飾をもつtRNAの試験管内翻訳活性。脱硫型tRNA修飾により、ウミシイタケルシフェラーゼの翻訳活性が低下した。ナノルシフェラーゼは脱硫型tRNA修飾の影響を受けないレポータータンパク質(注12)。
(B)脱硫型修飾をもつtRNAのアミノアシル化効率。
(C)脱硫型修飾をもつtRNAのリボソーム上におけるAAA/AAGコドンへの結合量。
有意差はそれぞれ***p<0.001, **p<0.01, *p<0.05。
さらに、脱硫型tRNA修飾(mcm5h2U)がコドン認識能を低下させる分子機構を解明するため、石黒 健介 特任助教は、理化学研究所の白水 美香子 チームリーダーらと共同で、リボソームと修飾状態の異なるtRNAとの複合体について、クライオ電子顕微鏡による構造解析を行いました(図3A、B)。その結果、mcm5h2UはAAAコドンとの対合において、水素結合が1本のみの不安定な塩基対を形成していることが明らかとなりました。この構造的特徴が、AAAコドンに対する認識能の低下を引き起こす要因であることが示されました(図3C)。一方で、AAGコドンとの対合においては、mcm5h2Uはmcm5s2Uと同じ対合様式でGを認識しているものの、硫黄がないため安定性が低下していることが示されました(図3C)。
これらの構造生物学的知見は、脱硫したtRNAがコドン解読能力を低下させる分子基盤を明確に示すものであり、翻訳制御におけるtRNA修飾の重要性を強く裏付ける成果です。

図3:リボソームのAサイト(注13)における脱硫型tRNA修飾によるコドン認識の構造解析
(A)Pサイト(注14)に大腸菌tRNAiMet(紫)、Aサイトにヒト細胞質tRNALys(緑)が結合した大腸菌70Sリボソームの原子モデル。
(B)ヒト細胞質tRNALys(緑)とAAAコドン(灰色)の塩基対合。16S rRNAの保存残基(黄緑)がコドン–アンチコドン二重鎖の副溝側から接触している。
(C)アンチコドン1字目(34位)のmcm5s2U(未処理)およびmcm5h2U(脱硫型修飾)とコドン3字目(AまたはG)との塩基対合。水素結合を赤点線で、その距離を赤字で示す。mcm5h2UはAとの対合において、水素結合が1本のみの不安定な塩基対を形成し、さらにGとの対合においても、硫黄がないため、対合の安定性が低下している。
〈今後の展望〉
今後は、脱硫型tRNA修飾の上昇を誘導する生理的条件や環境ストレスを特定し、その制御機構を明らかにすることを目指します。これにより、酸化ストレス応答における翻訳制御の新たな分子基盤を解明するとともに、ヒト疾患との関連についても明らかにしていきたいと考えています。
発表者・研究者等情報
東京大学大学院工学系研究科 化学生命工学専攻
莫 喩楓(Yufeng Mo) 博士課程
石黒 健介 特任助教
宮内 健常 特任研究員
鈴木 勉 教授
論文情報
雑誌名:Nature Communications
題 名:Translational Regulation by Oxidative Desulfuration of tRNA Modifications
著者名:Yufeng Mo, Kensuke Ishiguro, Kenjyo Miyauchi, Yuriko Sakaguchi, Yosei Hanzawa, Naho Akiyama, Ayaka Murayama, Kodai Machida, Hiroaki Imataka, Akio Yamashita, Takayuki Ohira, Mikako Shirouzu, and *Tsutomu Suzuki
* Corresponding author
DOI:10.1038/s41467-026-70126-7
URL:https://www.nature.com/articles/s41467-026-70126-7
研究助成
本研究は、日本学術振興会(JSPS)科学研究費助成事業の基盤研究(S)「RNA エピジェネティックスと高次生命現象」(代表:鈴木勉、JP26220205)および科学技術振興機構(JST)戦略的創造研究推進事業ERATO「鈴木RNA修飾生命機能プロジェクト」(研究総括:鈴木勉、JPMJER2002)などの支援を受けて実施されました。
用語解説
(注1)tRNA
Transfer RNA(転移RNA)。タンパク質合成において、コドン(特定の3塩基配列)とアミノ酸を1対1で対応させるアダプター分子として機能する。70~90塩基長の短い一本鎖RNAで、特徴的なクローバー葉状の二次構造をとり、さらに折りたたまれてL字型の立体構造を形成する。tRNAは3’末端に対応する特定のアミノ酸を結合し、20種類のアミノ酸それぞれに対して複数種類のtRNAが存在する。tRNAはコドンに対応する3塩基からなるアンチコドンをもち、リボソーム上でmRNA(messenger RNA、伝令RNA)のコドンと対合し、そのコドンに対応するアミノ酸を伸長中のタンパク質へと導入する。
(注2)酸化ストレス
細胞内で産生される活性酸素が、それを除去する抗酸化機構(抗酸化物質や抗酸化酵素)の能力を超えて過剰となり、細胞や組織に酸化的損傷を与える状態を指す。
(注3)アンチコドン
tRNAの34~36位(1~3字目)の3つの塩基から構成される配列。リボソーム上で対応するコドンと塩基対を形成することで遺伝暗号を解読し、対応するアミノ酸の導入を可能にする。
(注4)リボソーム
タンパク質合成の場となる巨大なRNAとタンパク質の複合体。複数種のリボソームRNA(rRNA)と多数のタンパク質から構成され、大小2つのサブユニットからなる。大サブユニットはペプチド転移反応を触媒し、小サブユニットはmRNAとtRNA間のコドン–アンチコドン対合の正確性を監視する。
(注5)コドン
遺伝暗号の基本単位。RNAの4種類の塩基(アデニン、グアニン、ウラシル、シトシン)が3つずつ並んだ配列で、64通りが存在する。標準的な遺伝暗号では、このうち61種が20種類のアミノ酸を指定し、残り3種はタンパク質合成の終結を指示する終止コドンである。
(注6)アミノアシル化
tRNAの3’末端にアミノ酸を結合させる反応。各アミノ酸に対して特異的なアミノアシルtRNA合成酵素が存在し、対応するtRNAに正しいアミノ酸を結合させることで、コドンとアミノ酸の対応関係が厳密に保証されている。
(注7)クライオ電子顕微鏡
生体分子試料を極低温(約−200℃)で急速凍結し、電子線を照射して構造を観察する電子顕微鏡法。水溶液中の状態をほぼ保持したまま解析できるため、生体内に近い構造情報を得ることが可能である。
(注8)転座反応
翻訳過程において、ペプチド結合形成後にリボソームがmRNA上を1コドン分移動する過程。これにより、AサイトおよびPサイトに結合していたtRNAが順次PサイトおよびEサイトへと移動する。英語ではtranslocationという。
(注9)RNA質量分析法
質量分析計を用いてRNA分子を解析する手法。RNAをヌクレオシド単位または短い断片に酵素分解し、液体クロマトグラフィーで分離した後、質量分析を行う。得られた質量電荷比(m/z)から精密分子量を決定し、修飾構造の同定や修飾率の計測を行うことができる。
(注10)衝突活性化解離
質量分析における断片化手法の1つ。イオン化した分子を希ガスと衝突させることで内部エネルギーを与え、分子を断片化させる。生成したフラグメントイオンのパターンを解析することで、分子の構造や修飾位置を詳細に決定できる。RNAの場合、配列と修飾部位の解析が可能。
(注11)ポリソーム画分
1本のmRNAに複数のリボソームが同時に結合して翻訳を行っている状態をポリソーム(polysome)という。細胞抽出液を密度勾配遠心法などで分画すると、翻訳中のmRNA–リボソーム複合体がポリソーム画分として分離される。一般的にこの画分に存在するtRNAは、実際に翻訳に参加していることを示す。
(注12)レポータータンパク質
化学発光や蛍光などで検出可能な酵素(例:ルシフェラーゼ)を発現させることにより、遺伝子発現やタンパク質合成活性を可視化・定量するために用いられるタンパク質のこと。
(注13)Aサイト
アミノアシルtRNAがmRNAのコドンを解読するために結合するリボソーム上の部位。
(注14)Pサイト
ぺプチジルtRNAが結合するリボソーム上の部位。
プレスリリース本文:PDFファイル
Nature Communications:https://www.nature.com/articles/s41467-026-70126-7
おすすめ記事
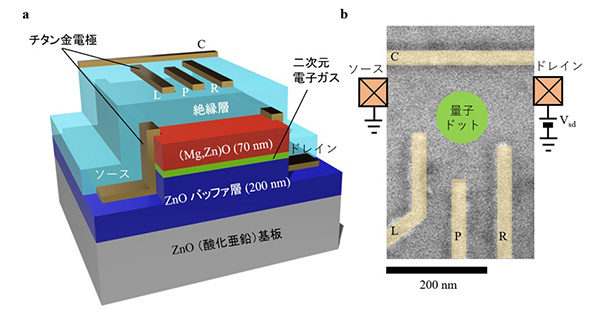
酸化亜鉛における電界制御量子ドット形成と量子多体効果観測を実現 ─新材料量子デバイス開発に期待─

セラミックスにおける新拡散メカニズムを発見 ―セラミックスの焼結メカニズムの解明と新たな粒界設計指針の構築―


