1.発表者:
岡村 梢(東京大学 大学院工学系研究科 化学システム工学専攻 博士課程)
バドラ サラ(東京大学 大学院工学系研究科 化学システム工学専攻 特任助教)
村上 聖(次世代バイオ医薬品製造技術研究組合 専務理事)
杉山 弘和(東京大学 大学院工学系研究科 化学システム工学専攻 教授)
2.発表のポイント:
◆モノクローナル抗体製造の培養工程について、細胞増殖・抗体産生・代謝・不純物生成を同時かつ精度良く記述できる新規数理モデルを構築しました。
◆物質収支に基づく物理モデルと、広範な実験情報で精度を高めるデータ駆動型モデルを融合させた、ハイブリッドモデルを開発しました。モデルパラメータの寄与度分析により、更なる精度向上や適用範囲拡大に向けた指針を得ることを可能にしました。
◆本モデルは、生産性や不純物等の品質を同時に考慮した動的シミュレーションを可能にし、デジタル化による迅速なプロセス設計や製品上市に貢献します。
3.発表概要:
東京大学大学院工学系研究科化学システム工学専攻の岡村梢大学院生、バドラ サラ特任助教、杉山弘和教授、次世代バイオ医薬品製造技術研究組合の村上聖専務理事らの研究グループは、モノクローナル抗体(Monoclonal antibody:mAb)(注1)の製造で中核をなす培養工程について、細胞増殖・抗体産生・代謝・不純物生成を同時に、精度良く記述できる新規数理モデルを構築しました。
バイオ医薬品の有効成分として代表的なmAbは、遺伝子改変した細胞株(注2)に目的となる抗体を産生させ、これを分離・精製することで製造されます。本研究では、細胞の培養工程を対象に、物質収支を基礎とする物理モデル(注3)と、広範な実験データで計算精度を高めるデータ駆動型モデル(注4)を図1のように融合させた、ハイブリッドモデル(注5)を構築しました。これにより、生産性や代謝活性の高い新規細胞株であっても、乳酸のような代謝物濃度の急激な変化を記述できるようになりました。さらに、宿主細胞由来タンパク質(Host cell protein:HCP)(注6)やDNAのような工程由来不純物に関して新たな物理モデルを定義し、生産性だけでなく品質も考慮したシミュレーションを可能にしました。
本研究により、培養工程のより高度な設計と制御、ひいてはバイオ医薬品製造におけるデジタル技術のさらなる活用が期待されます。特に、生産性と品質面を同時にシミュレーション可能にしたことは、製薬産業のニーズに応えるものであり、デジタル化のより一層の促進に向けた重要な貢献となります。今後は、モデルの適用範囲拡大や、さまざまな意思決定への応用に向けて、研究をさらに展開していきます。
本研究成果は、2022年9月29日(米国太平洋夏時間)に米国学術誌「Industrial & Engineering Chemistry Research」のオンライン版(オープンアクセス)で公開されました。
4.発表内容:
① 研究背景
バイオ医薬品の有効成分として代表的なmAbは、抗がん剤からCOVID-19の治療まで幅広く使われており、その市場は近年、急速に拡大しています。mAbは、遺伝子改変した細胞株に目的となる抗体を産生させ、これを分離・精製することで製造されます。培養工程は製造プロセス全体の中核であり、細胞株や運転方式を始めとするさまざまな技術が盛んに開発されています。全ての選択肢を実験的に検討することは、もはや困難なレベルに達しており、シミュレーションによる評価や最適化が必要になってきています。しかし、生物現象は複雑であり、シミュレーションに必要な数理モデルの構築はそもそも容易ではありません。特に、近年開発される細胞株には、生産性や代謝活性が非常に高いものもあり、従来のモデルでは細胞の増殖や代謝などの動的挙動をうまく記述できないケースが出てきます。さらに、製薬産業ではプロセスの高純度化に向けて、死細胞の溶出に伴う工程由来不純物の生成が問題視されていますが、これに至っては数理モデルが未確立なのが現状です。
本研究では、これらの課題の解決に向けて、細胞増殖・抗体産生・代謝・不純物生成を同時かつ精度良く記述できる、新規数理モデルの構築に挑みました。数理モデルには一般に、自然科学法則に基づく物理モデルと、データ的裏付けに基づくデータ駆動型モデルの二つがあります。本研究では、これらをハイブリッドモデルとして統合することで、両者のメリットを引き出すことを試みました。さらに、不純物についても新たなモデルを構築し、細胞増殖・代謝と連動させることで、生産性のみならず品質面も考慮した動的シミュレーションを可能にすることを目指しました。
② 研究内容と成果
東京大学杉山弘和教授らは、mAbの製造について、数理モデルとシミュレーションを用いたプロセス設計や運転支援の手法を研究してきました。次世代バイオ医薬品製造技術研究組合(MAB組合)村上聖らは、品質基準Good Manufacturing Practice(GMP)(注7)に準拠した製造実験設備である神戸GMP集中研で、次世代製造技術の開発と実証に取り組んできました。本研究は、培養・精製・製剤化からなるmAb製造プロセスのうち、Chinese Hamster Ovary(CHO)細胞(注8)を培養し、抗体を産生させる培養工程を対象としました(図2)。研究は、杉山教授らが2021年に発表した培養モデル[1]を基盤とし、MAB組合神戸GMP集中研で取得した製造実験データを活用して進められました。
構築したモデルは3つのモジュールから成ります(図3)。第1モジュールは、既報[1]に基づいて、細胞増殖・抗体産生・代謝を、物質収支式とMonodの式(注9)で記述した物理モデルです。第2モジュールにはデータ駆動型モデルが組み込まれており、これが第1モジュールの計算結果を修正していきます。用いられるのは、pHや温度、溶存酸素濃度など、第1モジュールで考慮されていなかった培養環境に関するパラメータで、これらをフル活用することで、グルコースや乳酸といった代謝物濃度の精度を向上させます。修正された計算結果は、第3モジュールに入力され、死細胞密度が計算されるとともに、本研究で新規提案する物理モデルによって、死細胞の溶出に伴うHCP及びDNA濃度の時間変化を求めることができます。
本研究の独自性として、次の4点が挙げられます。第1に、全体をハイブリッドモデルとしたことにより、従来は困難だった細胞増殖・抗体産生・代謝・不純物生成を同時に記述できるようになった点があります(図4)。モデルは、mAb製造に広く用いられているCHO-K1細胞株に加え、MAB組合で新規開発された高生産性CHO-MK細胞株にも適用でき、フェドバッチ培養(注10)・パーフュージョン培養(注11)の両方を記述できることが示されました。第2に、死細胞の溶出を考慮し、それに伴うHCPとDNAの生成を表した物質収支式を新たに定義した点があります。これにより、生産性に加えて品質面も考慮した動的シミュレーションが可能になりました。第3に、ハイブリッドモデル上で、モデルパラメータの寄与度分析を可能にした点があります。データ駆動型モデルは専ら、生物学的解釈が困難という課題がありますが、これを乗り越えるために施した独自の工夫です。実際、乳酸濃度の変化に重要な役割を果たす変数や、変数同士の関係性に対する知見が得られ、今後のさらなるモデル精度向上や適用範囲拡大に向けた指針が得られました。第4に、ハイブリッドモデルを構築する際に、物理モデルを基盤、データ駆動型モデルを補助として、それぞれ役割を与えた点も挙げられます。物理モデルの枠組みに収まらなかった実験情報も、データ駆動型モデルがパラメータとして取り込むことで、有効活用が可能になっています。プロセス理解に立脚しつつ、データをフル活用していくための、新しい仕組みとして位置づけられます。
③ 今後の展望
本研究により、培養工程のより高度な設計と制御、ひいてはバイオ医薬品製造におけるデジタル技術のさらなる活用が期待されます。特に、生産性と品質面を同時にシミュレーション可能にしたことは、製薬産業のニーズに的確に応えるものであり、デジタル化のより一層の促進に向けた重要な貢献です。今後は、モデルの適用範囲拡大や、さまざまな意思決定への応用に向けて、研究をさらに展開していきます。
5.研究支援:
本研究は、AMED次世代治療・診断実現のための創薬基盤技術開発事業「国際競争力のある次世代抗体医薬品製造技術開発/バイオ医薬品製造プロセスの先端的シミュレーション技術の開発」課題JP21ae0121015(代表:杉山弘和)、課題JP21ae0121016(代表:山本修一)、AMED次世代治療・診断実現のための創薬基盤技術開発事業「バイオ医薬品の高度製造技術の開発/高度バイオ医薬品製造プロセスの設計フレームワーク」課題JP18ae0101064(代表:杉山弘和)、「バイオ医薬品の高度製造技術の開発/バイオ医薬品製造技術の実証研究」課題JP18ae0101058(代表:村上聖)の研究として行われたものです。
6.発表雑誌:
雑誌名:「Industrial & Engineering Chemistry Research」(オンライン版:9月29日・オープンアクセス)
論文タイトル:Hybrid modeling of CHO cell cultivation in monoclonal antibody production with an impurity generation module
著者:Kozue Okamura, Sara Badr*, Sei Murakami, Hirokazu Sugiyama
* Corresponding author
DOI番号:10.1021/acs.iecr.2c00736
7.参考文献:
[1] Badr, S.; Okamura, K.; Takahashi, N.; Ubbenjans, V.; Shirahata, H.; Sugiyama, H. Integrated design of biopharmaceutical manufacturing processes: operation modes and process configurations for monoclonal antibody production. Computers and Chemical Engineering, 2021, 107422.
8.用語説明:
(注1) モノクローナル抗体(Monoclonal antibody:mAb):動物の免疫システムでは、体内に侵入した細菌などの異物(抗原)を検知すると「抗体」と呼ばれるタンパク質が作られる。モノクローナル抗体は、抗原にある目印(抗原決定基)のうち、特定の一種類とだけ結合する抗体を人工的に増殖させたものである。モノクローナル抗体を有効成分とする抗体医薬品は、抗原抗体反応を利用してガンや新型コロナウイルス感染症(COVID-19)などの疾病の治療に用いられる。(参考:国立がん研究センター https://ganjoho.jp/public/qa_links/dictionary/dic01/modal/mAb.html)
(注2) 細胞株:起源となるヒト、動物、微生物の細胞を体外でも無限に増殖できるようにしたもののことを指す。単一の細胞プールから分注された均一な組成の容器を集め、状態一定の条件下で保存しているものを「セル・バンク」と呼び、細胞株はバンク化することが可能である。(参考:独立行政法人医薬品医療機器総合機構 https://www.pmda.go.jp/files/000156150.pdf)
(注3) 物理モデル:物理・化学・生物学的な原理に基づいて記述されるモデルを指す。現象をよく捉えられている限り、信頼性が高く、外挿性に優れるという利点がある。「メカニスティックモデル」「ファンダメンタルモデル」「ホワイトボックスモデル」とも呼ばれる。(参考:Narayanan, et al., 2019, https://doi.org/10.1002/bit.27097)
(注4) データ駆動型モデル:モデルの入出力関係のみに基づいて記述されるモデルを指す。モデル化したい現象の機構について限られた理解しかない中でも、良質なデータが十分にあれば容易にモデルを構築しうるという利点がある。「統計モデル」「ブラックボックスモデル」とも呼ばれる。(参考:Narayanan, et al., 2019, https://doi.org/10.1002/bit.27097)
(注5) ハイブリッドモデル:物理モデルとデータ駆動型モデルを組み合わせたモデルを指す。精度を高めつつ、解釈可能性を維持することを目的としている。「グレイボックスモデル」とも呼ばれる。(参考:Narayanan, et al., 2019, https://doi.org/10.1002/bit.27097)
(注6) 宿主細胞由来タンパク質(Host cell protein:HCP):抗体医薬品製造における各工程由来の不純物のうち、細胞基材に由来する、目的物質以外のタンパク質の総称である。(参考:独立行政法人医薬品医療機器総合機構 https://www.pmda.go.jp/files/000156781.pdf)
(注7) Good Manufacturing Practice(GMP):医薬品及び医薬部外品の製造管理及び品質管理の基準のことを指す。日本では、薬事法に基づいた「医薬品及び医薬部外品の製造管理及び品質管理の基準に関する省令」により定められている。(参考:厚生労働省 https://www.mhlw.go.jp/web/t_doc_keyword?keyword=%E5%93%81%E8%B3%AA%E7%AE%A1%E7%90%86%E3%81%AE%E5%9F%BA%E6%BA%96&dataId=81aa6647&dataType=0&pageNo=1&mode=0)
(注8) Chinese Hamster Ovary(CHO)細胞:チャイニーズハムスターの卵巣由来の細胞を指す。モノクローナル抗体を始めとする組換えタンパク質生産における実績や構築の容易さなどから、現在商用化されている抗体医薬品の製造に、最も広く用いられている宿主細胞の一つである。(参考:大政健史, 2021, https://www.jstage.jst.go.jp/article/seibutsukogaku/99/1/99_99.1_15/_pdf)
(注9) Monod(モノー)の式:Jacques Monodによって提唱された、微生物が増殖する速度を栄養成分濃度で表した式を指す。式の形は酵素の反応速度を表すMichaelis-Menten(ミカエリス・メンテン)の式をもとにしているが、Monodの式は実験から経験的に得られた式である。(参考:Jacques Monod, 1949, https://doi.org/10.1146/annurev.mi.03.100149.002103)
(注10) フェドバッチ培養:栄養成分を含む新鮮培地を培養中に加えていく運転方式のことを指す。生産培養では最も広く用いられている方式である。流加培養とも呼ばれる。(参考:村上聖, 2019, https://www.sbj.or.jp/wp-content/uploads/file/sbj/9706/9706_tokushu_5.pdf)
(注11) パーフュージョン培養:新鮮培地を供給するとともに、細胞を残しながら液体のみを抜き出して装置内の液量を一定に保つ運転方式のことを指す。灌流培養とも呼ばれる。(参考:村上聖, 2019, https://www.sbj.or.jp/wp-content/uploads/file/sbj/9706/9706_tokushu_5.pdf)
9.添付資料: 図1 ハイブリッドモデルのイメージ(発表論文から抜粋)。「Fundamental model」が物理モデルに、「Data-driven model」がデータ駆動型モデルに、それぞれ対応している。
図1 ハイブリッドモデルのイメージ(発表論文から抜粋)。「Fundamental model」が物理モデルに、「Data-driven model」がデータ駆動型モデルに、それぞれ対応している。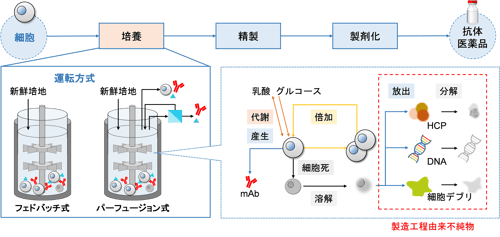 図2 培養工程と主要な現象の概略図(発表論文から抜粋・翻訳)
図2 培養工程と主要な現象の概略図(発表論文から抜粋・翻訳)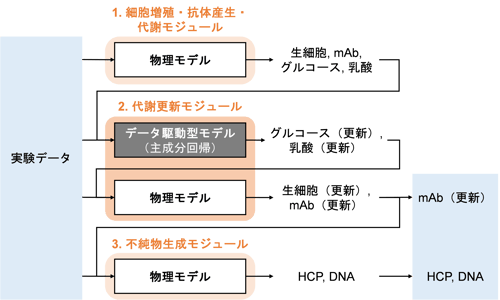 図3 ハイブリッドモデルのモジュール構造(発表論文から抜粋・翻訳)
図3 ハイブリッドモデルのモジュール構造(発表論文から抜粋・翻訳)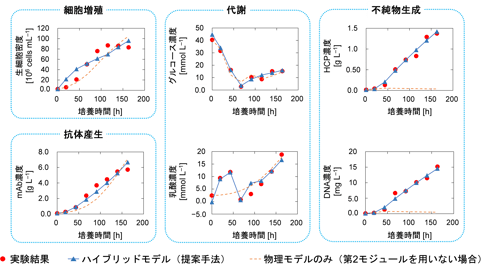 図4 モデル適用結果の一例(発表論文から抜粋・翻訳)。
図4 モデル適用結果の一例(発表論文から抜粋・翻訳)。
代謝物、とりわけ乳酸濃度の精度が向上したことで、不純物生成の計算が可能になった。
プレスリリース本文:PDFファイル
Industrial & Engineering Chemistry Research:https://pubs.acs.org/doi/10.1021/acs.iecr.2c00736
おすすめ記事
モノクローナル抗体のつくる責任、つかう責任を定量化〜抗体医薬品の製造に伴う環境影響と、治療による健康効果を評価〜


