◆発表のポイント
・代表的な難治がんである膵がんでは、がん細胞周囲の「線維化(1)」が、薬剤のがん細胞への到達に対する「障壁」となり、治療成績を悪化させます。
・膵がんの「線維化」を試験管内で再現する独自の立体培養技術を駆使し、「線維化障壁」が形成されるメカニズムを解析しました。
・線維化障壁形成に関与するタンパク質ROCK2の同定に成功し、今後、膵がんにおける「線維化障壁」を克服し、治療成績を改善するための足掛かりとなることが期待されます。
岡山大学学術研究院ヘルスシステム統合科学学域の狩野光伸教授、岡山大学学術研究院医歯薬学域(薬)の田中啓祥助教、東北大学大学院医学系研究科の正宗淳教授、東京大学大学院工学系研究科のカブラル・オラシオ准教授らの研究グループは、膵がんの特徴であり難治化の原因である「線維化障壁」の形成にタンパク質ROCK2が関与することを明らかにしました。これらの研究成果は2024年3月29日、科学雑誌「Journal of Controlled Release」に掲載されました。
多くのがんの治療成績が近年改善している中で、膵がんの5年生存率は未だ1割ほどに留まっています。膵がんが難治である原因として、がん細胞周囲に特徴的に認められる「線維化」があります。線維化は、薬剤のがん細胞への到達を阻む障壁となり、膵がんの治療成績を悪化させます。これまで「線維化障壁」を実験的に再現することは難しく、詳細なメカニズムの解析は困難でした。
本研究では、独自の立体培養技術を駆使して、線維化障壁形成メカニズムの解析に挑み、タンパク質ROCK2の関与を突き止めました。本研究成果は、既に他の疾患での適応を目的として開発が進んでいるROCK2に対する薬剤の利用による「線維化障壁」の克服の可能性を示唆するもので、膵がんの治療成績の改善を実現していく足掛かりとなることが期待されます。
◆研究者からのひとこと

■発表内容
<現状>
膵がんは代表的な難治がんであり、線維化が特徴です。線維化は、血液中の各種の薬剤が、がん細胞へと到達するのを阻む障壁となることが、これまでの研究より明らかとなっています。したがって、こうした「線維化障壁」の克服戦略を確立することが、膵がんの治療成績を改善するうえで重要です。しかし、線維化障壁を実験的に再現することは難しく、どのように線維化障壁が形成され、どのようにすれば治療することができるのか、これまで不明でした。
<研究成果の内容>
本研究では、独自技術を用いて膵がん患者由来の線維芽細胞(2)を立体培養(3)しました。構築した立体組織では、コラーゲン等の線維性タンパクが沈着し、それに伴い薬剤を模した物質が通過しにくくなることが認められました。こうして試験管内に再現することに成功した「線維化障壁」を詳しく解析し、タンパク質ROCK2が線維化において認められるコラーゲンの過剰沈着等の異常過程に関わることを見出しました。また、ROCK2を標的化することで、線維化障壁を克服しうることを明らかにしました。
<社会的な意義>
膵がんの5年生存率は未だ1割ほどで、罹患率も世界的に増加傾向にあります。ゆえに、膵がんの難治化の原因を明らかにし、克服することは極めて重要な社会的課題です。本研究では、膵がんの難治化への関与が明らかとされながらも、有効な治療法が未確立であった「線維化障壁」のメカニズム解析を行いました。線維化障壁形成への関与を明らかにしたROCK2は、既に他の疾患での適応を目指し薬剤の開発が進んでいます。本研究成果は、これら既存薬剤を用いた線維化障壁克服の可能性を示唆するとともに、線維化障壁の形成メカニズムとその克服法の詳細な解析を可能とする実験基盤を確立したことで、膵がんの新たな治療戦略開発の足掛かりとなることが期待されます。
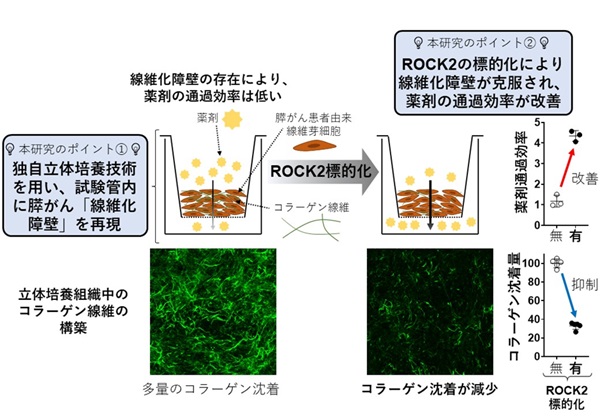
図:独自立体培養技術を利用することにより本研究で確立した試験管内の膵がん「線維化障壁」の模式図(上段)、作成した線維化組織中のコラーゲン線維沈着の様子を示した顕微鏡写真(下段)。タンパク質ROCK2を標的化(左が標的化なし、右が標的化あり)することで、コラーゲン沈着量が減少し、薬剤通過効率が改善する。ROCK2標的化によって、薬物通過効率は約4倍増加、コラーゲン沈着量は約6割減少した(右グラフ)。
■論文情報
論 文 名:Targeting ROCK2 improves macromolecular permeability in a 3D fibrotic pancreatic cancer microenvironment model
掲 載 紙:Journal of Controlled Release
著 者:Hiroyoshi Y. Tanaka, Takuya Nakazawa, Takuya Miyazaki, Horacio Cabral, Atsushi Masamune, Mitsunobu R. Kano
D O I:10.1016/j.jconrel.2024.03.041
U R L:https://www.sciencedirect.com/science/article/pii/S0168365924001949?dgcid=author
■研究資金
本研究は、科研費(JP23H02653, JP22H03051, JP 26293119, JP23K06279, JP20K16989)、公益財団法人 日本膵臓病研究財団、公益財団法人 両備檉園記念財団、公益財団法人 稲盛財団、公益財団法人 薬学研究奨励財団、公益財団法人 山陽放送学術文化・スポーツ振興財団、公益財団法人 川崎医学・医療福祉学振興会の支援を受けて実施しました。
■補足・用語説明
(1)線維化:過剰に増殖した線維芽細胞(下記用語(2)参照)と、これら細胞が多量に分泌したコラーゲン等の線維性のタンパク質が沈着した病的な状態。膵がんの特徴であり、がん細胞を取り囲むように線維化が存在する(線維化により形成される「海」の中に膵がん細胞の「島」が点在しているような状態)。
(2)線維芽細胞:線維化において過剰な増殖が認められる紡錘状の細胞で、コラーゲン等の線維性のタンパクを分泌する。正常な状態では臓器・組織の適度な強度の維持に重要な役割を果たすが、線維化ではコラーゲン等の分泌が過剰となり、臓器・組織の硬化を引き起こす。
(3)立体培養:従来の培養細胞実験は、プラスチック製のシャーレ「平面」上で実施されていたが、こうした平面培養の実験系では、線維化障壁のような「立体的」な構造を再現することができない。立体培養技術は、体内の環境を平面培養に比べてよりよく再現することを可能とする技術群の総称で、動物実験を補完・代替する実験技術として近年注目されている。
プレスリリース本文:PDFファイル
Journal of Controlled Release:https://www.sciencedirect.com/science/article/pii/S0168365924001949?dgcid=author
おすすめ記事
神経抑制に役立つタンパク質の巧みな光応答メカニズムを解明

ミトコンドリアとメラノソームの接触がメラニン色素形成を制御 −メラニン色素形成を支える細胞内機構を解明−