発表のポイント
◆ 微細加工技術や細胞極性制御技術を駆使することで、培養肝細胞が分泌した胆汁成分を細胞外へと連続的に排泄させ、さらにそれらを非侵襲的に回収することが可能な新規肝細胞培養デバイスを開発しました。◆ 本手法により、従来の肝細胞培養法による非連続的かつ侵襲的な胆汁回収方法と比較して、13.7倍高い濃度での胆汁排泄代謝物の回収に成功しました。
◆ このように培養肝細胞からの連続的な胆汁排泄を可能にしたことは、in vitroにおける肝臓の生理機能の再現に向けた極めて大きなブレイクスルーであり、創薬研究や肝疾患研究への応用が高く期待されます。

培養肝細胞が分泌した胆汁成分の連続的排泄を可能とする新規肝細胞培養デバイス
概要
東京大学大学院工学系研究科の酒井 康行 教授、西川 昌輝 准教授、時任 文弥 特任研究員、同大学大学院薬学系研究科の楠原 洋之 教授、名古屋市立大学大学院薬学研究科の荒川 大 教授、金沢大学医薬保健研究域薬学系の加藤 将夫 教授、三井化学株式会社新事業開発センター細胞培養ソリューション室の山崎 聡 室長らによる研究グループは、培養肝細胞が分泌する胆汁成分をマイクロ流路(注1)へ連続的に排泄させ、さらにそれらを非侵襲的に回収することに世界で初めて成功しました。
本研究では、微細加工技術(注2)や密着結合タンパク質による肝細胞極性の制御技術を駆使することで、従来の培養法では極めて困難であった細胞外への連続的な胆汁排泄と、その非侵襲的回収を可能にしました。さらに本手法により、従来の肝細胞培養法による非連続的かつ侵襲的な胆汁回収法と比較して、13.7倍という高い濃度で胆汁排泄代謝物を回収することに成功しました。
このように培養肝細胞からの連続的な胆汁排泄を可能とすることは、in vitro(注3)での肝生理機能の再現に向けた大きなブレイクスルーであり、創薬研究や肝疾患研究への多大な貢献が期待されます。
発表内容
胆汁排泄は生体恒常性の維持に不可欠な肝機能の一つであり、肝細胞で産生される胆汁は脂質消化やコレステロール代謝、薬物および代謝産物の排泄において重要な役割を担っています。一般に、ヒトにおける胆汁排泄の評価は侵襲的で困難なため、この胆汁排泄プロセスを忠実に再現できるin vitroヒト肝培養モデルは、薬物動態研究や肝疾患研究において極めて有用なツールとして期待されています。しかしながら、従来の肝細胞培養法では、分泌された胆汁の排泄出口が存在しないため、胆汁は毛細胆管(注4)内あるいは胆管様組織内に蓄積するのみであり、生体肝組織のように胆汁成分を細胞・組織外部へと連続的に排泄させることは極めて困難でした。
今回本研究グループは、微細加工技術を駆使することで、培養肝細胞が排泄した胆汁成分をマイクロ流路内へ連続的に排泄させ、さらにそれらを回収することが可能な新規肝細胞培養デバイスを開発しました(図1)。本デバイスの培養部表面にはマイクロ流路(幅:3 µm、高さ:10 µm)が高密度にパターニングされており、肝細胞が分泌した胆汁成分はその流路へと排泄され、中央の胆汁回収ポートへと輸送される仕組みになっています。また、本デバイスを三井化学株式会社の酸素透過培養プレート(InnoCell®)上に設置することで、肝細胞へ十分な酸素供給が可能になり、これにより毛細胆管の形成が促進します。

図1:本研究で作製した肝細胞培養デバイス
(A)培養デバイスの外観。(B)市販セルカルチャープレートへの本培養デバイスの設置。(C)デバイス培養表面に成型されたマイクロ流路の走査型電子顕微鏡(SEM)画像。
実際に本デバイス上でラット初代肝細胞やヒト肝細胞(PXB-cells®およびHepaSH®)を培養し、蛍光標識された胆汁酸を曝露したところ、マイクロ流路への胆汁酸の連続的な排泄が確認され(図2A)、それらを胆汁回収ポートで回収することに成功しました。さらに、ラットおよびヒト肝細胞が分泌した内因性胆汁酸の回収にも成功し、両者の間における胆汁酸組成の種差についても観測されました(図2B)。加えて、デバイスの培養表面に肝密着結合タンパク質であるclaudin-1(注5)を被覆することで、本来は隣接する肝細胞間に閉鎖的に形成される胆管腔を、肝細胞と培養表面の間に形成させることに成功しました(図3A)。これにより、マイクロ流路側への胆汁代謝物の排泄量は1.8倍に向上しました。さらに、従来の胆汁回収手法では、多量の回収液により胆汁排泄代謝物が希釈されてしまうという問題がありましたが、本デバイスを用いることで、13.7倍という極めて高い濃度での回収に成功しました(図3B)。
このように培養肝細胞から連続的に胆汁成分を排泄させることが可能な培養系は世界的にも前例がなく、in vitroでの肝生理機能再現への大きなブレイクスルーといえます。今回の成果は、今後の創薬研究や肝疾患研究へ多大な貢献をもたらすものと期待されます。
なお、本研究は東京大学ライフサイエンス研究倫理支援室の承認のもと実施されました。

図2:マイクロ流路内への胆汁排泄と回収した胆汁酸のヒトとラット間の種差
(A)マイクロ流路内への蛍光標識胆汁酸の排泄。赤矢印はマイクロ流路内へ排泄された蛍光標識胆汁酸を示す。(B)デバイスを用いたヒトおよびラット肝細胞培養における胆汁回収ポート内の胆汁酸組成。CA:コール酸、TCA:タウロコール酸、GCA:グリココール酸、CDCA:ケノデオキシコール酸、TCDCA:タウロケノデオキシコール酸、GCDCA:グリコケノデオキシコール酸。

図3:Claudin-1による肝細胞極性制御と胆汁排泄代謝物の高濃度回収
(A)デバイス培養表面へのclaudin-1被覆による“開いた”毛細胆管腔形成促進の観測。(B)従来の侵襲的胆汁回収法と本デバイスを用いた胆汁回収法における胆汁排泄代謝物の回収濃度比較。
〇関連情報:
「酸素透過培養プレート(InnoCell®)による毛細胆管形成促進に関する論文」(2024/2/21)
Comparative analysis of bile canaliculi formation in fresh and flask-delivered human hepatocytes from humanized mouse livers under sufficient oxygen supply, F. Tokito, Y. Gong, D. A. Kurniawan, S. Kaneko, H. Shioda, S. Lee, A. Kushima, M. Inamatsu, C. Tateno, H. Choi, M. Nishikawa, Y. Sakai, Fundamental Toxicological Sciences, 11(1), 17-25 (2024)
「claudin-1を用いた“開いた”毛細胆管腔形成に関する論文」(2023/8/22)
Induction of open-form bile canaliculus formation by hepatocytes for evaluation of biliary drug excretion, H. Arakawa, Y. Nakazono, N. Matsuoka, M. Hayashi, Y. Shirasaka, A. Hirao, I. Tamai, Communications Biology, 6(1):866 (2023)
発表者・研究者等情報
東京大学
大学院工学系研究科
酒井 康行 教授
西川 昌輝 准教授
時任 文弥 特任研究員
伊藤 大知 教授
稲垣 奈都子 准教授
大学院薬学系研究科
楠原 洋之 教授
名古屋市立大学 医薬学総合研究院 大学院薬学研究科
荒川 大 教授
金沢大学 医薬保健研究域 薬学系
玉井 郁巳 教授:研究当時
現:同大学名誉教授
加藤 将夫 教授
増尾 友佑 准教授
三井化学株式会社
新事業開発センター 細胞培養ソリューション室
山崎 聡 室長
楊 晶晶 チームリーダー
研究本部 先端材料・ソリューション研究所
江刺家 勝弘 チームリーダー
論文情報
雑誌名:Cell Reports Physical Science
題 名:Continuous Bile Excretion from Polarized Hepatocytes on a Microchannel-Patterned Device
著者名:Fumiya Tokito, Hiroshi Arakawa, Yuya Nakazono, Mikito Kiyofuji, Yang Liang, Fukino Kono, Mathieu Danoy, Hyunjin Choi, Ya Gong, Katsuhiro Esashika, Jingjing Yang, Satoshi Yamasaki, Natsuko F. Inagaki, Taichi Ito, Kenpei Tai, Hiroyuki Kusuhara, Yusuke Masuo, Yukio Kato, Ikumi Tamai, Takeshi Katsuda, Masaki Nishikawa, and Yasuyuki Sakai
DOI:10.1016/j.xcrp.2026.103229
URL:https://www.cell.com/cell-reports-physical-science/fulltext/S2666-3864(26)00135-9
研究助成
本研究は、AMED再生医療・遺伝子治療の産業化に向けた基盤技術開発事業(再生医療技術を応用した高度な創薬支援ツール技術開発)の「オンチップ灌流型MPSを基礎とした肝と他臓器が関与する薬物動態・毒性の予測系開発」(課題番号:22be1004201h0001)」、AMED再生医療等実用化研究事業の「ヒト肝オルガノイドを利用したMASLD/MASH治療薬の開発研究(課題番号:25bk0104189h0001)」、AMED生命科学・創薬研究支援基盤事業(BINDS)「新規薬効成分の薬物動態解析と体内動態特性予測の支援(課題番号:JP25ama121051)」、JST研究成果最適展開支援プログラム(A-STEP)「接着タンパク質を利用した新規胆汁排泄評価手法の開発(体系的番号:JPMJTR24UC)」、JSPS科研費「胆汁成分の連続回収が可能なin vitro肝細胞培養系の開発(課題番号:JP23KJ0541)」の支援により実施されました。
用語解説
(注1)マイクロ流路:微細加工技術を用いて、プラスチックやゴムなどの基板上に作製された微細な管のこと。液体を精密に流し、混合、反応、分離などの化学・バイオ操作を極小スケールで行うために用いられる。
(注2)微細加工技術:材料の表面や内部に、マイクロメートル単位(1 mmの1000分の1)の極小かつ精密な形状・構造を形成する技術。
(注3)in vitro:「試験管内で(の)」。試験管内や培養器などの人工的な環境を指す。
(注4)毛細胆管:隣接した肝細胞同士の間に形成され、肝細胞が分泌した胆汁が流れる管。
(注5)claudin-1:肝細胞を含む上皮細胞において、細胞同士を強固に密着させ、細胞間の隙間をシールする膜タンパク質の一種。
プレスリリース本文:PDFファイル
Cell Reports Physical Science:https://www.cell.com/cell-reports-physical-science/fulltext/S2666-3864(26)00135-9
おすすめ記事
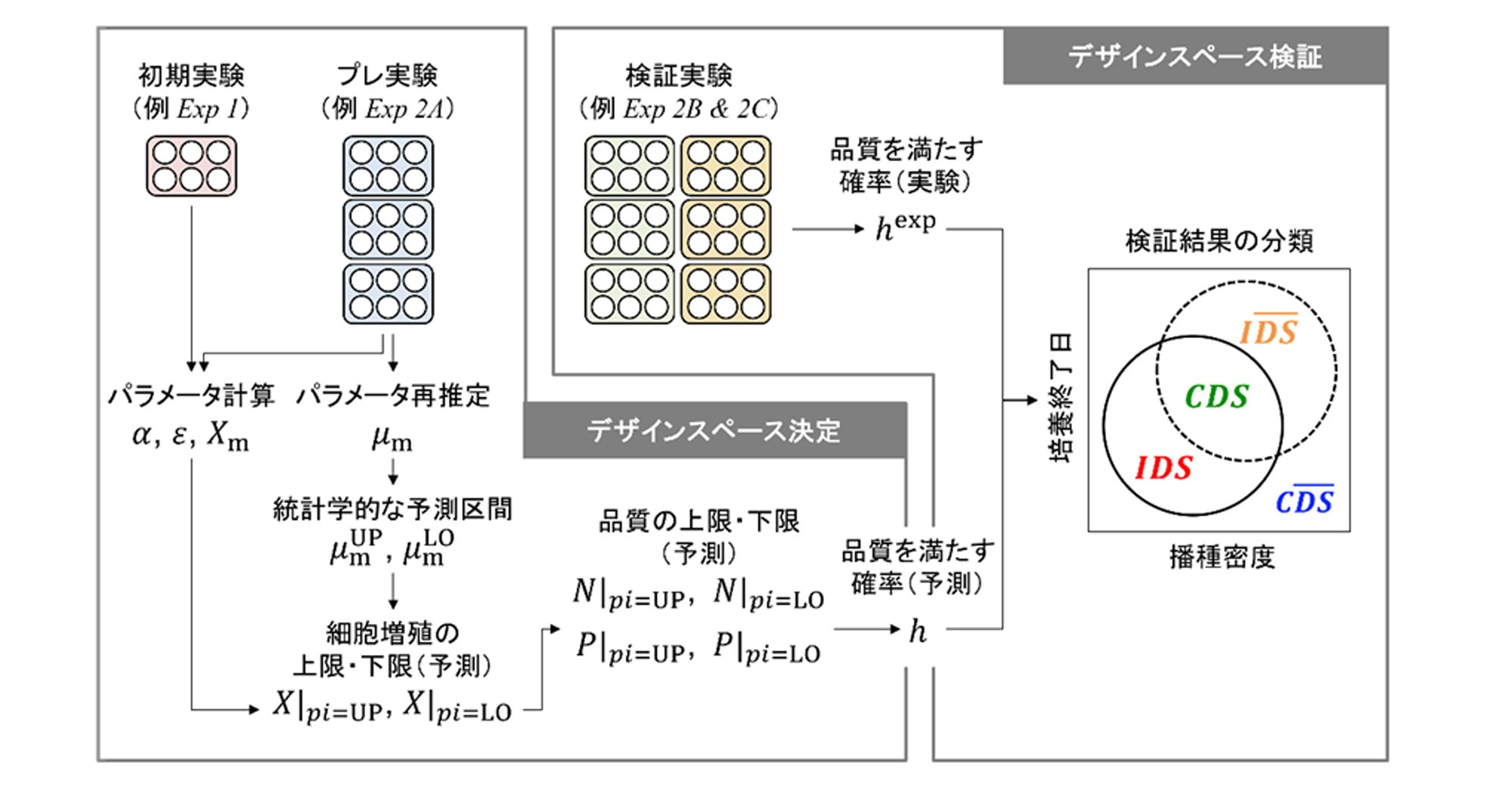
再生医療向け幹細胞培養のプロセス設計をデジタル化 ―数理モデルに基づくデザインスペースを実験的に検証―


