発表のポイント
◆ 分子設計により化学シフトを自在に制御する新戦略を確立し、生体内で複数の酵素活性を同時に可視化できる超核偏極MRI分子プローブ群の開発に成功しました。
◆ 開発した分子プローブを用いて、抗がん剤スニチニブ治療に伴う酵素活性の変化を腫瘍サイズの変化に先立って検出し、治療効果の早期判定が可能であることを実証しました。
◆ 本手法は、腫瘍の高精度分類や治療モニタリングに加え、さまざまな疾患における画像診断への応用が期待されます。
 本発表の概要
本発表の概要
(Adapted from the Journal of the American Chemical Society 2026,
DOI: 10.1021/jacs.5c16910)
概要
東京大学大学院工学系研究科の谷田部 浩行 助教、齋藤 雄太朗 助教、山東 信介 教授、量子科学技術研究開発機構(QST)の齋藤 圭太 主任技術員、小池 歩 研究員、高草木 洋一 グループリーダー、岐阜大学のAbdelazim Elsayed Elhelaly特任講師、兵藤 文紀 教授、松尾 政之 教授、大阪大学量子情報・量子生命研究センターの水上 渉 教授、東京大学先端科学技術研究センターの菅谷 麻希 博士研究員、大澤 毅 准教授、米国国立衛生研究所の山本 和俊 上級研究員、Murali Cherukuri Krishna主任研究員らの研究グループは、生体内で同時に複数の酵素活性を計測可能な超核偏極MRI分子プローブ群(注1、2)を合理設計し、生体内のアミノペプチダーゼ活性の同時検出に世界で初めて成功しました。
レニン–アンジオテンシン系の代謝反応を触媒するアミノペプチダーゼは、血管新生や腫瘍成長に深く関与する酵素群であり、それらの生体内における活性バランスを直接評価する方法の開発は、疾患診断や治療効果判定において重要な課題でした。超核偏極は、核磁気共鳴法(NMR/MRI)(注3)の検出感度を飛躍的に高める量子センシング技術(注4)として注目されていますが、超核偏極状態の寿命が数十秒に限られていることや、高感度化に適した分子構造に制約があることから、これまで生体内で同時に解析できる分子種や酵素反応は限定的でした。特に、多重解析を行うためには、十分に長い高感度化時間を維持しつつ、NMR/MRI スペクトル上にて各分子プローブとそれらの代謝産物とが互いに重ならないNMR/MRI信号を与える、つまりはすべての成分が異なる化学シフト(注5)を示して完全に分離できるような分子設計が求められていました。
研究グループは、量子化学計算と実験的評価を統合した分子設計戦略により、酵素反応性を担う分子構造要素と、NMR/MRI信号の化学シフトを制御する分子構造要素を分離・最適化しました。その結果、複数の超核偏極MRI分子プローブを同時に使用しても、それぞれの代謝反応を生体内で識別可能な分子プローブ群を開発しました。さらに、これらを用いてモデルマウスの腫瘍内における複数のアミノペプチダーゼ活性の同時検出に成功し、抗血管新生薬スニチニブ治療に伴う酵素活性変化を、腫瘍サイズの変化に先立って検出できる可能性を示しました。
本研究で確立した分子設計原理と超核偏極MRI多重解析技術は、複数の酵素活性の同時検出に基づいて高精度かつ非侵襲的に病態を評価するための新しい画像診断技術の開発基盤として、その応用展開が期待されます。
本研究成果は2026年2月26日(米国太平洋時間)に米国化学会が出版する科学誌「Journal of the American Chemical Society」オンライン版に掲載されました。
発表内容
レニン–アンジオテンシン系に関連するアミノペプチダーゼ群は、血管新生や循環機能の制御に重要な役割を果たしています。これらの酵素活性のバランスは、がんや腎疾患をはじめとするさまざまな疾患と密接に関連していることが知られており、生体内で複数のアミノペプチダーゼ活性を同時に評価することは、病態の理解や高精度診断において重要な課題とされてきました。しかし、これまでの方法では、血液や尿などを体外で調べる間接的な解析に限られており、腫瘍の中などの特定の場所におけるアミノペプチダーゼ活性のバランスを直接捉えることは困難でした。
生体内で分子の代謝反応、すなわち酵素活性を非侵襲的に検出する手法として、核磁気共鳴法(NMR/MRI)とその検出感度を飛躍的に向上させる量子センシング技術である超核偏極を組み合わせた超核偏極MRIが注目されています。一方で、高感度化されたNMR/MRI信号は時間とともに不可逆的に減衰するため、超核偏極MRI分子プローブには十分に長い高感度化時間と速やかな酵素反応性が同時に求められます。さらに、酵素活性の多重解析を行うためには、複数の分子プローブおよびその代謝産物が互いに重ならない化学シフトを示す必要があり、これが分子設計上の大きな制約となっていました。
本研究では、量子化学計算と実験的評価を統合した分子設計戦略により、ジペプチドを基盤骨格として、酵素反応性を規定するN末端構造とNMR/MRI信号の化学シフトを制御するC末端構造を独立に最適化しました。その結果、十分に長い高感度化時間を維持しつつ、分離した化学シフトを示す複数の超核偏極MRI分子プローブの開発に成功しました。これらの分子プローブを超偏極装置 SpinAligner(QST 量子生命科学研究所に設置された国内1号機)を用いて同時に高感度化し、尾静脈より速やかにマウスに投与することで、生体内における複数のアミノペプチダーゼ活性の同時検出・可視化に世界で初めて成功しました。
さらに、本手法を腫瘍モデルマウスに適用し、抗血管新生薬スニチニブ治療に伴うアミノペプチダーゼ活性の変化を解析しました。その結果、腫瘍体積の変化が観測される以前の段階で、アミノペプチダーゼ活性の低下を検出できることを示し、治療効果の早期判定における有用性を実証しました。また、複数の分子プローブを組み合わせて評価することで、単一の分子プローブを用いるよりも、腫瘍タイプの分類が高精度に実現できる可能性も示しました。

図1:本発表の概要
(Adapted from the Journal of the American Chemical Society 2026,
DOI: 10.1021/jacs.5c16910)
本研究で開発した生体内アミノペプチダーゼ活性の多重解析を実現する分子プローブ群は、がん診断のみならず、腎疾患や神経変性疾患など、多様な疾患の診断における臨床応用が期待されます。また、本研究で確立した化学シフトを制御する超核偏極MRI分子プローブの設計原理は、他の酵素を標的とした分子プローブの多重解析を実現するための指針としても貢献していくことが期待されます。
発表者・研究者等情報
東京大学
大学院工学系研究科
谷田部 浩行 助教
齋藤 雄太朗 助教
山東 信介 教授
先端科学技術研究センター
菅谷 麻希 博士研究員
大澤 毅 准教授
量子科学技術研究開発機構 量子生命科学研究所
高草木 洋一 グループリーダー
兼務:千葉大学 量子生命構造創薬センター (cQUEST) 連携教授
齋藤 圭太 主任技術員
小池 歩 研究員
岐阜大学
大学院医学系研究科
Abdelazim Elsayed Elhelaly 特任講師
兵藤 文紀 教授
松尾 政之 教授
大阪大学 量子情報・量子生命研究センター
水上 渉 教授
米国国立衛生研究所 国立癌研究所
Murali Cherukuri Krishna 主任研究員
山本 和俊 上級研究員
論文情報
雑誌名:Journal of the American Chemical Society
題 名:In vivo multiplexed analysis of aminopeptidase activities by hyperpolarized molecular probes for tumor diagnostic applications
著者名:Hiroyuki Yatabe, Keita Saito, Ayumi Koike, Yoichi Takakusagi, Abdelazim E. Elhelaly, Fuminori Hyodo, Masayuki Matsuo, Wataru Mizukami, Maki Sugaya, Tsuyoshi Osawa, Kazutoshi Yamamoto, Murali C. Krishna, Yutaro Saito, Shinsuke Sando*
DOI:10.1021/jacs.5c16910
URL:https://doi.org/10.1021/jacs.5c16910
研究助成
本研究は、文部科学省「光・量子飛躍フラッグシッププログラム(Q-LEAP)」(JPMXS0120330644)、JSPS 科研費 基盤研究(A)(研究代表者:山東信介、JP19H00919)、若手研究(研究代表者:齋藤雄太朗、JP20K15396)、特別研究員奨励費(研究代表者:谷田部浩行、JP22J22617)、基盤研究(B) (研究代表者:高草木洋一、JP23K27561;兵藤文紀、23H02621)、研究活動スタート支援(研究代表者:齋藤圭太、JP23K19228)、JST創発的研究支援事業(研究代表者:高草木洋一、JPMJFR225G;兵藤文紀、JPMJFR2168)、文部科学省共同利用・共同研究システム形成事業~学際領域展開ハブ形成プログラム~(JPMXP1323015488) の支援を受けて実施されました。
用語解説
(注1)超核偏極技術
核磁気共鳴法の検出感度を劇的に向上させる量子センシング技術。超核偏極技術の中で最も広く使われている動的核偏極法では、核磁気共鳴法の検出対象となる安定同位体で標識された分子(分子プローブ)と、偏極源となる安定ラジカル分子をガラス状態の溶媒中で混合し、極低温・高磁場下にてマイクロ波を照射することで、核磁気共鳴法の検出感度が向上した超高感度化状態を作り出す。
(注2)分子プローブ
分子の置かれた周辺環境やその変化、化学反応などを引き金として、信号を変化させる分子。
(注3)核磁気共鳴法
外部磁場中の核スピンに対してラジオ波を照射することにより核スピンの置かれた環境に関する情報を取得する技術。NMRと略される。その中でも、画像化技術である核磁気共鳴イメージング法(MRI)は非侵襲的な画像診断技術として広く用いられている。
(注4)量子センシング技術
量子性を利用して、物質や環境のさまざまな物理量を計測する技術。古典的な計測技術の感度や精度の限界を超えた超高感度な計測を実現できる。
(注5)化学シフト
核磁気共鳴法で観測される信号の周波数を表す指標。分子の構造や周囲の環境によって信号の位置が少しずつずれるため、複数の分子が同時に存在していても、それぞれを別々の信号として見分けることができる。
プレスリリース本文:PDFファイル
Journal of the American Chemical Society:https://doi.org/10.1021/jacs.5c16910
おすすめ記事
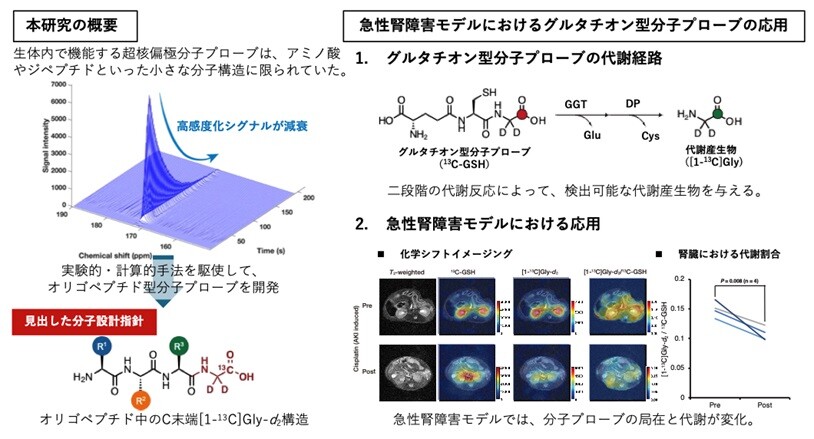
量子センシング技術を活用した生体内における代謝反応の直接計測 ―急性腎障害のモデルマウスにおける腎臓での代謝反応の可視化に成功―


